Chúng tôi rất vui mừng chia sẻ kiến thức về từ khóa Oxit axit la gi và hi vọng rằng nó sẽ hữu ích cho các bạn đọc. Bài viết tập trung trình bày ý nghĩa, vai trò và ứng dụng của từ khóa trong việc tối ưu hóa nội dung trang web và chiến dịch tiếp thị trực tuyến. Chúng tôi cung cấp các phương pháp tìm kiếm, phân tích và chọn lọc từ khóa phù hợp, kèm theo các chiến lược và công cụ hữu ích. Hi vọng rằng thông tin chúng tôi chia sẻ sẽ giúp bạn xây dựng chiến lược thành công và thu hút lưu lượng người dùng. Cảm ơn sự quan tâm và hãy tiếp tục theo dõi blog của chúng tôi để cập nhật kiến thức mới nhất.
Oxit axit là gì? tính chất hóa học của oxit axit trong hóa học lớp 8 ra sao? Đây là thắc mắc gửi nhiều nhất cho VIETCHEM trong kỳ thi học kỳ và Trung học Phổ Thông vừa qua. Hãy cùng chúng tôi đi tìm hiểu rõ ràng và cụ thể về oxit axit, tính chất và bài tập có lời giải rõ ràng và cụ thể trong nội dung bài viết tiếp sau đây.
Bạn Đang Xem: Oxit axit là gì? Tính chất hóa học và hướng dẫn bài tập … – VietChem
1. Khái niệm oxit axit là gì?
Oxit axit còn được gọi là anhidrit axit, đây là các loại oixt có tác dụng với bazơ tạo thành muối hóa học, tác dụng với nước tạo thành axit. Oxit axit thường là của phi kim, tác dụng được với nước sẽ tạo ra các sản phẩm axit tương ứng. Oxit axit gồm hai yếu tố hóa học, trong này sẽ có một yếu tố là oxi.
Công thức tổng quan là: MaOb.

Khái niệm oxit axit là gì?
2. Cách gọi tên oxit axit

Cách đọc tên oxit axit trong hóa học
Tên oxit axit: (Tên tiền tố chỉ số nguyên tử của phi kim) + Tên phi kim + (tên tiền tố chỉ số nguyên tử oxi) + ‘‘Oxit’’
Chỉ số
Tên tiền tố
Ví dụ
1
Mono (không cần đọc khi đối chiếu với các hợp chất thông thường)
ZnO: Kẽm oxit
2
Đi
UO2: Urani đioxit
3
Tri
SO3: Lưu huỳnh trioxit
4
Tetra
5
Penta
N2O5: Đinitơ pentaoxit
6
Hexa
7
Hepa
Mn2O7: Đimangan heptaoxit
3. Oxit có những loại nào?
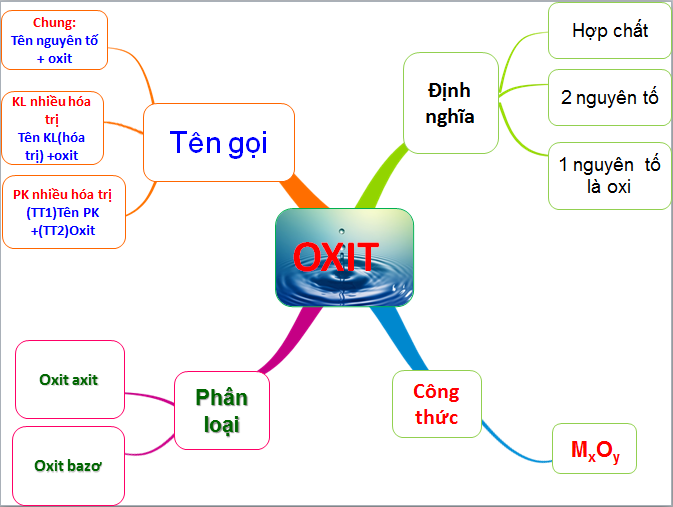
Phân loại oixt trong hóa học
3.1. Oxit bazơ
Đây là những loại oxit tác dụng được với axit để tạo thành muối và nước. Một số oxit bazơ phản ứng với nước để tạo thành bazơ tan gọi là kiềm.
- Ví dụ: Na2O – NaOH, Fe2O3 – Fe(OH)3…
3.2. Oxit axit
Đây là những oxit tác dụng với bazo để tạo ra muối và nước, phản ứng với nước tạo thành một axit.
- Ví dụ: Mn2O7 – HMnO4, CO2 – H2CO3, P2O5 – H3PO4.
3.3. Oxit lưỡng tính
Là loại oxit có thể tác dụng với axit hoặc bazơ để tạo muối và nước.
- Ví dụ: Al2O3, ZnO.
3.4. Oxit trung tính
Đây là oxit không phản ứng với nước để tạo bazơ hay axit, không phản ứng với bazơ hay axit để tạo muối.
- Ví dụ: Cacbon monoxit – CO, Nitơ monoxit – NO,…
4. Tính chất hóa học của oxit axit
4.1. Oxit axit có tính tan
Trừ SiO2 thì hồ hết các oxit axit đều tan trong nước để tạo thành dung dịch axit.
Ví dụ:
SO3 + H2O → H2SO4
P2O5 + 3H2O → 2H3PO4
N2O5 + H2O → 2HNO3
SO2 + H2O→ H2SO3
4.2. Oxit axit tác dụng với nước H2O
Phần lớn các loại oxit axit khi tác dụng với nước H2O sẽ tạo ra dung dịch axit trừ SiO2.
SO3 + H2O → H2SO4
CO2 + H2O→ H2CO3 (Phản ứng thuận nghịch)
4.3. Tác dụng với oxit bazo tan để tạo ra muối
Thông thường đó là các oxit tác dụng được với nước (Na2O, CaO, K2O, BaO)
SO3 + CaO -> CaSO4
P2O5 + 3Na2O -> 2Na3PO4

Các tính chất hóa học của oxit axit
4.4 Tác dụng với bazơ tan
Xem Thêm : Focus group là gì? Cập nhật ngay những tin tức về focus group
Bazo tan là bazo của kim loại kiềm và kiềm thổ mới. Cụ thể, có 4 bazo tan như sau: NaOH, Ca(OH)2, KOH, Ba(OH)2.
P2O5 + 6KOH → 2K3PO4 + 3H2O
Tuỳ vào tỉ lệ mol giữa oxit axit và bazơ tham gia phản ứng mà sản phẩm tạo ra sẽ khác nhau, có thể là nước + muối trung hoà, muối axit hoặc hỗn hợp 2 muối.
- Gốc axit tương ứng có hoá trị II
So với kim loại trong bazơ có hoá trị I:
Tỉ lệ mol bazo và oxit axit là một trong những: Phản ứng tạo muối axit
NaOH + SO2→ NaHSO3
Tỉ lệ mol bazo và oxit axit là 2: Phản ứng tạo muối trung hoà
2KOH + SO3 → K2SO3 +H2O
- So với kim loại trong bazơ có hoá trị II
Tỉ lệ mol bazo và oxit axit là một trong những: Phản ứng tạo muối trung hoà
CO2 + Ca(OH)2 → CaCO3
Tỉ lệ mol bazo và oxit axit là 2: Phản ứng tạo muối axit
SiO2 + Ba(OH)2 → BaSiO3
- So với axit có gốc axit hoá trị III
So với kim loại có hoá trị I:
Tỉ lệ mol bazo và oxit axit là 6:
P2O5 + 6NaOH → 2Na2HPO4 +H2O
Tỉ lệ mol bazo và oxit axit là 4:
P2O5 + 4NaOH → 2NaH2PO4 +H2O
Tỉ lệ mol bazo và oxit axit là 2:
P2O5 + 2NaOH +H2O → 2NaH2PO4
4.5. Oxit lưỡng tính
Là loại oxit có thể tác dụng với axit hoặc bazơ để tạo muối và nước.
Ví dụ: Al2O3, ZnO.
4.6. Oxit trung tính
Đây là oxit không phản ứng với nước để tạo bazơ hay axit, không phản ứng với bazơ hay axit để tạo muối.
Ví dụ: Cacbon monoxit – CO, Nitơ monoxit – NO,…
5. Các dạng bài tập oxit axit tác dụng với bazo
5.1. Trường hợp 1
Lúc các oxit axit (CO2, SO2…) tác dụng với dung dịch kiềm (KOH, NaOH…)
Phương trình hóa học
CO2 + NaOH → NaHCO3 (1)
CO2 + 2NaOH → Na2CO3 + H2O (2)
Cách giải
Bước 1: Xét tỉ lệ mol bazo và oxit axit, giả sử là T
– Nếu T ≤ 1: Sản phẩm thu được là muối axit tức chỉ xẩy ra phản ứng (1)
– Nếu 1 < T < 2: Sản phẩm thu được là muối axit và muối trung hòa tức xẩy ra song song 2 phản ứng (1) và (2)
– Nếu T ≥ 2: Sản phẩm thu được là muối trung hòa tức chỉ xẩy ra phản ứng (2).
Bước 2: Viết phương trình phản ứng và tính toán theo phương trình đó (nếu xẩy ra cả hai phản ứng thì nên đặt ẩn và giải theo hệ phương trình)
Bước 3: Tính toán theo yêu cầu của đề bài đã cho

Các dạng bài tập oxit axit thường gặp trong hóa học lớp 8
5.2. Trường hợp 2
Lúc các oxit axit (CO2, SO2…) tác dụng với dung dịch kiềm thổ (Ca(OH)2, Ba(OH)2…)
Phương trình phản ứng
CO2 + Ca(OH)2 → CaCO3 + H2O (1)
2CO2 + Ca(OH)2 → Ca(HCO3)2 (2)
Cách giải
Bước 1: Xét tỉ lệ
– Nếu T ≤ 1: Sản phẩm thu được là muối trung hòa (xẩy ra phản ứng (1))
– Nếu 1 < T < 2: Sản phẩm thu được là muối axit và muối trung hòa (xẩy ra phản ứng (1) và (2))
– Nếu T ≥ 2: Sản phẩm thu được là muối axit (xẩy ra phản ứng (2)).
Bước 2 và bước 3 tương tự trường hợp 1.
6. Bài tập oxit axit có lời giải
Bài tập hóa học có lời giải rõ ràng và cụ thể
Bài tập 1: Tiến hành sục khí CO2 ở tham gia tiêu chuẩn vào trong 1 lượng dư dung dịch Ca(OH)2. Hãy tính khối lượng kết tủa thu được sau phương trình phản ứng.
Lời Giải:
Theo đề bài ta tính được nCO2 = 5,6/22,4 = 0,25 mol
Ca(OH)2 dư nên ta có phương trình phản ứng sau:
Xem Thêm : Yoni có nghĩa là gì? Linga là gì?
CO2 + Ca(OH)2 → CaCO3↓ + H2O
0,25 → 0,25 → 0,25
Từ phương trình ta có n CaCO3 = 0,25 mol => m CaCO3 = 100 x 0,25 = 25 gam
Tóm lại: Sau phản ứng ta thu được kết tủa có khối lượng 25 gam.
Bài tập 2: Tiến hành dẫn 2,24 lít khí SO2 ở tham gia tiêu chuẩn vào 150 ml dung dịch NaOH 1 M. Hãy tính nồng độ mol của những chất dung dịch có trong phản ứng.
Lời Giải:
Theo đề bài ta có nSO2 = 2,24/22,4 = 0,1 mol, nNaOH = CM.V = 1 x 0,15 = 1,15 mol
Phương trình phản ứng
SO2 + 2NaOH → Na2SO3 + H2O (1)
0,1 0,15
0,075 0,15 0,075
Từ phương trình ta thấy SO2 dư nên số mol sẽ tính theo NaOH
=> nNa2SO3 = 0,2 (mol)
CO2 + Na2SO3 + H2O → 2NaHSO3 (2)
0,025 0,075
0,025 0,025 0,05
Theo phương trình (2) ta thấy NaHSO3 dư nên sẽ tính theo số mol của SO2
nNaHSO3 = 2nSO2 = 0,025.2 = 0,05 (mol) => m = 5,2 (gam)
nNa2SO3 dư = 0,075 – 0,025 = 0,05 (mol) => m = 6,3 (gam)
Bài tập 3: Tiến hành đốt cháy hoàn toàn 8 gam lưu huỳnh, sản phẩm khi được sinh ra sẽ tiến hành hấp thụ hoàn toàn vào 500 ml dung dịch Ba(OH)2 0,4M thu được kết tủa X và dung dịch Y. Khi đu nóng dung dịch Y ta thu được m gam kết tủa. Hãy tính giá trị của m.
Lời Giải:
Theo đề bài ta tính được nS = 8/32 = 0,25 ml; nBa(OH)2 = 0,4 X 0,5 = 0,2 ml
S + O2 → SO2
0,25 0,25
SO2 + Ba(OH)2 → BaSO3↓ + H2O (1)
0,25 0,2
Theo phương trình (1) ta thấy SO2 dư 0,05 mol => nBaSO3 = 0,2 (mol)
SO2 + BaSO3 + H2O → Ba(HSO3)2 (2)
0,05 0,2
Theo phương trình (2) ta thấy BaSO3 dư nên số mol sẽ tiến hành tính theo SO2
Vậy ta có kết tủa Y nBaSO3 dư = 0,2 – 0,005 = 0,15 mol
Bài tập 4: Sục 6,72 lít khí CO2 trong tham gia tiêu chuẩn vào 400ml dung dịch NaOH 1M. Tính khối lượng muối tạo thành.
Giải
Ta có: nCO2 = 6,72 x 22,4 = 0,3 (mol)
nNaOH = CM x V = 1 x 0,4 = 0,4 (mol)
Phương trình hóa học
CO2 + 2NaOH → Na2CO3 + H2O (1)
Có: 0,3mol 0,4mol
Phường/ứ: 0,2vàlt;- 0,4 -> 0,2
Theo PTHH (1) ta thấy CO2 dư nên số mol tính theo NaOH tức nNa2CO3 = 0,2 (mol)
nCO2 p/ứ = 0,2 (mol) => nCO2 dư = 0,3 – 0,2 = 0, 1 (mol)
CO2 dư : CO2 + Na2CO3 + H2O → 2NaHCO3 (2)
Có : 0,1mol 0,2mol
Phường/ứ: : 0,1 -> 0,1 -> 0,2
Theo PTHH (2) ta thấy Na2CO3 dư nên số mol tính theo CO2:
nNaHCO3 = 2nCO2 = 0,1 x 2 = 0,2 (mol)
nNa2CO3dư = 0,2 – 0,1 = 0,1 (mol)
Dung dịch thu được sau phản ứng gồm 2 muối: Na2CO3 (0,1 mol), NaHCO3 (0,2 mol)
mNa2CO3 = 0,1 x 106 = 10,6 (g)
mNaHCO3 = 0,2 x 84 = 16,8 (g)
Trên đây là những thông tin về oxit axit mà Hóa chất VIETCHEM muốn san sớt đến độc giả. Hy vọng thông qua đó các bạn đã biết được oxit axit là gì? cách gọi tên, tính chất hóa học và cách giải bài tập oxit axit tác dụng với bazo ra sao?. Nếu như khách hàng nào có thắc mắc về oxit, vui lòng liên hệ với chúng tôi bằng phương pháp điền thông tin vào hộp thoại tương trợ trực tuyến 24/7 để được trả lời tốt nhất.
>>>XEM THÊM: : Silicon có ô nhiễm không? Những thông tin cấp thiết về chúng



