Chúng tôi rất vui mừng chia sẻ kiến thức về từ khóa So e hoa tri la gi để tối ưu hóa nội dung trang web và tiếp thị trực tuyến. Bài viết cung cấp phương pháp tìm kiếm, phân tích từ khóa và chiến lược hiệu quả. Cảm ơn sự quan tâm và hãy tiếp tục theo dõi để cập nhật kiến thức mới.
Electron hóa trị là một chuyên đề quan trọng và được quan tâm trong Khóa học Hóa Học Trung học phổ thông. Vậy electron hóa trị là gì? Cách xác định hóa trị của không ít yếu tố như nào? Hãy cùng thapgiainhietliangchi đi tìm hiểu cụ thể chi tiết về electron hóa trị trong nội dung bài viết tại chỗ này!
Bạn Đang Xem: Electron hóa trị là gì? Cách xác định hóa trị của các nguyên tố
Electron hóa trị là gì?
Khái niệm electron hóa trị là gì? Electron hóa trị (hay electron ngoài cùng) là những electron nằm ở các orbital ngoài cùng và hoàn toàn có thể tham gia vào các liên kết của nguyên tử.
Electron hóa trị các yếu tố nhóm chính sẽ nằm ở lớp ngoài cùng, trong yếu tố nhóm phụ (hay kim loại chuyển tiếp) electron hóa trị sẽ sở hữu tại lớp ngoài cùng và lớp d kề cận.

Các electron hóa trị đó chính là một phần của hồ hết các phản ứng hóa học vì chúng chứa năng lượng nhiều hơn so với những điện tử có trong các quỹ đạo bên trong.
Electron hóa trị của không ít yếu tố có thể tham gia vào liên kết của nguyên tử (nên gọi là electron liên kết) nhưng nó cũng có thể có thể không.
Số e hóa trị là gì? Số electron hóa trị là gì? Nói một cách đơn giản khác số electron hóa trị của một yếu tố sẽ đã cho thấy số electron tối đa có thể tham gia vào liên kết của nguyên tử yếu tố đó.
Đặc điểm của electron hóa trị là gì?
- Các electron khi tham gia vào liên kết hóa học và các phản ứng của nguyên tử. Nó sẽ tiến hành cho là chiếm các obitan có trong nguyên tử.
- Số electron hóa trị của nguyên tử có thể xác định được dựa trên bảng tuần hoàn hóa học vì chúng bằng với số trật tự nhóm của nguyên tử đó. Nguyên tử sẽ bền nhất nếu như chúng có lớp vỏ hóa trị chứa đầy các electron.
- Khi đối chiếu với các yếu tố phân nhóm chính, electron hóa trị sẽ chỉ tồn tại ở lớp electron nằm ngoài cùng.
- Một electron hóa trị hoàn toàn có thể tồn tại ở lớp vỏ bên trong của kim loại chuyển tiếp.
- Một nguyên tử nếu như đã đủ electron hóa trị thường sẽ bị trơ về mặt hóa học, có nghĩa nó ít hay là không tham gia vào các phản ứng hóa học khác nữa.
- Một electron hóa trị hoàn toàn có thể hấp thụ hay phóng thích năng lượng dưới dạng một photon.
- Các electron hóa trị cũng giúp ta xác định được độ dẫn điện của một yếu tố. Tùy thuộc vào thực chất này của không ít yếu tố mà yếu tố đó có thể là kim loại, phi kim.

Cách xác định Electron hóa trị
Xem Thêm : BitShares là gì? Tổng quan về đồng tiền ảo BitShare (BTS)
Electron hóa trị là gì và cách xác định số electron hóa trị như nào? Xác định được số electron hóa trị ở lớp ngoài cùng của một yếu tố hóa học đó chính là một kỹ năng cấp thiết cho quá trình học Hóa lên rất cao. Dựa vào đó chúng ta có thể biết được số liên kết trong phân tử, cơ sở của việc phân tử đó hình thành nên liên kết đôi chứ không phải liên kết đơn.
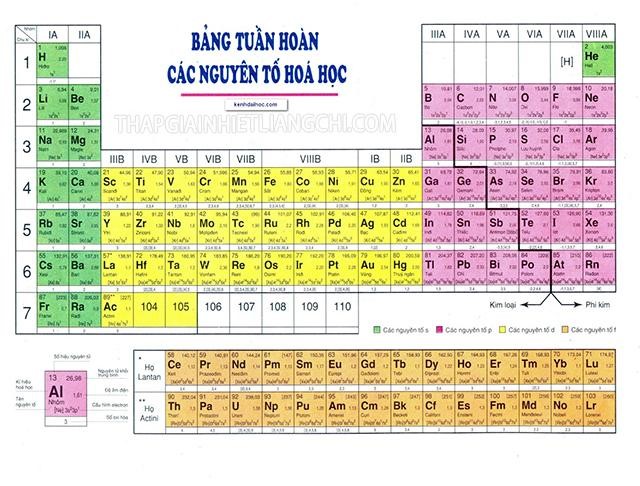
Ta có thể xác định số electron hóa trị dựa vào bảng khối hệ thống tuần hóa học các yếu tố hóa học. Dựa vào bảng HTTH các yếu tố hóa học đó chính là cách đơn giản để xác định số electron hóa trị của một yếu tố.
Xem thêm: Phản ứng Este hóa là gì? Đặc điểm, tính hiệu suất phản ứng Este hóa
Bảng khối hệ thống tuần hoàn Hóa học của Mendeleev được chia làm 18 cột hay gọi là các nhóm. Ta có nhóm như IA, IIA, IIIA… hay IB, IIB, IIIB…
Số electron hóa trị của một yếu tố sẽ trùng với số trật tự của nhóm. Các yếu tố thuộc cùng một cột, một nhóm thì sẽ sở hữu cùng electron hóa trị.

Các yếu tố thuộc nhóm A thì sẽ sở hữu số electron hóa trị là số electron ở lớp ngoài cùng của yếu tố. Các yếu tố thuộc nhóm B thì sẽ sở hữu số electron hóa trị có thể nằm ở phân lớp ngoài cùng hoặc là ở sát phân lớp ngoài cùng (nếu như phân lớp này chưa bão hòa) của yếu tố. Cụ thể như sau:
- Các yếu tố thuộc nhóm IA sẽ sở hữu 1e hóa trị
- Các yếu tố thuộc nhóm IIA sẽ sở hữu 2e hóa trị
- Các yếu tố thuộc nhóm IIIA sẽ sở hữu 3e hóa trị
- Các yếu tố thuộc nhóm IVA sẽ sở hữu 4e hóa trị
- Các yếu tố thuộc nhóm VA sẽ sở hữu 5e hóa trị
- Các yếu tố thuộc nhóm VIA sẽ sở hữu 6e hóa trị
- Các yếu tố thuộc nhóm VIIA sẽ sở hữu 7e hóa trị
- Các yếu tố thuộc nhóm VIIIA sẽ sở hữu 8e hóa trị
Ví dụ : Xác định số e hóa trị của Crom. S và Cr đều thuộc nhóm VI nên sẽ sở hữu tối đa 6e hóa trị. Cụ thể như sao:
Xem Thêm : Sứ Mệnh Là Gì? Ý Nghĩa Sứ Mệnh Của Doanh Nghiệp
– S có cấu hình e như sau: 1s2 2s2 2p6 3s2 3p4. Số e hóa trị thuộc orbitan hóa trị lớp ngoài cùng là 3s2 3p4
– Cr có cấu hình e như sau: 1s2 2s2 2p6 3s2 3p6 3d5 4s1. Số e hóa trị của Crom thuộc orbitan phân ở lớp ngoài cùng và sát ngoài cùng là 3d5 4s1.
Một số điều cần lưu ý về e hóa trị
Một lưu ý bạn phải phải đặc biệt quan trọng quan tâm đến đó là số electron hóa trị sẽ hoàn toàn khác biệt với hóa trị của nguyên tử yếu tố.
Hóa trị của yếu tố là gì? Hóa trị là của một yếu tố sẽ tiến hành xác định bằng chính số liên kết hóa học mà một nguyên tử của yếu tố này đã tạo nên trong phân tử. Hóa trị của một yếu tố sẽ đặc trưng cho khả năng của nguyên tử yếu tố đó có thể hình thành nên một số liên kết hóa học nhất định (khi xét cho từng phân tử hay hợp chất cụ thể khác nhau).
Hóa trị của yếu tố không thể xác định được dựa vào bảng tuần hoàn được. Mà phải ghi nhận rõ cấu trúc phân tử của một chất ta mới có thể xác định được hóa trị của không ít yếu tố đã cấu trúc nên chất đó.
Thực tế thì không phải bao giờ ta cũng sẽ xác định được cấu trúc phân tử của một chất cả. Vì vậy mà các nhà khoa học đã đề xuất ra khái niệm hóa trị hình thức hay gọi là số oxy hóa (nhằm mục tiêu xác định hóa trị giả thiết và tương đối của nguyên tử).
Giữa số oxy hóa của yếu tố và số electron hóa trị của nguyên tử lại sở hữu mối liên hệ mật thiết. Số oxy hóa dương lớn số 1 của một yếu tố sẽ bằng với số electron hóa trị của nó.
Nội dung bài viết trên là những tri thức về electron hóa trị, hy vọng rằng sau khoản thời gian tham khảo nội dung bài viết các bạn đã nắm được electron hóa trị là gì, cách xác định hóa trị hay phân biệt được hóa trị của yếu tố là gì với electron hóa trị. Đây là vấn đề tri thức quan trọng giúp các bạn tiếp thu tốt hơn các tri thức Hóa học sau này, chính vì thế nên dành nhiều thời kì để học tập nghiên cứu.


