Liên kết cộng hóa trị là gì? Đấy là một trong những liên kết hóa học cơ phiên bản thường thấy. Vậy người đã biết gì về chúng? Nội dung bài viết tiếp sau đây sẽ hỗ trợ người có thêm những thông tin cụ thể về khái niệm, phân loại cùng tính chất của nó.
Liên kết cộng hóa trị là gì?
Liên kết cộng hóa trị (LKCHT) được hiểu là liên kết giữa hai nguyên tử hay ion trong đó những cặp electron (e) sẽ tiến hành share với nhau. Nó còn được gọi là liên kết phân tử, được hình thành giữa hai nguyên tử phi kim có mức giá trị của độ âm điện tương tự hoặc tương đối gần nhau.
Chúng được tìm thấy trong nhiều hóa học, ví dụ như những gốc và đại phân tử. Thuật ngữ này được tận dụng lần trước tiên vào năm 1939, tuy nhiên từ thời điểm năm 1919 Irving Langmuir đã tìm ra khái niệm “cộng hóa trị” để mô tả sống lượng electron được share từ những nguyên tử phụ cận.
Những hợp chất có LKCHT rất có thể ở trạng thái khí, lỏng hoặc rắn. Mỗi cặp e được share giữa hai nguyên tử được gọi là cặp liên kết, trái lại nếu không được share sẽ gọi là cặp đơn độc.
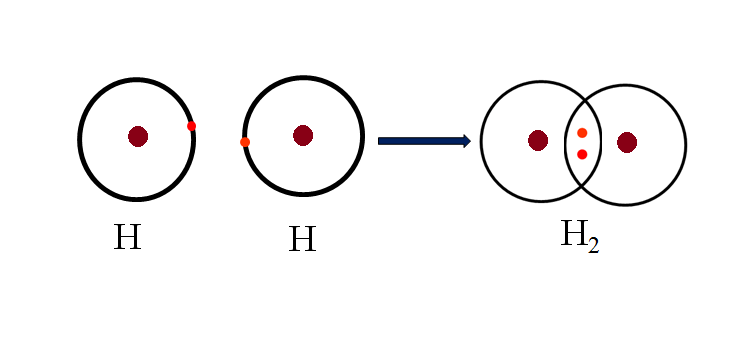
Liên kết cộng hóa trị là gì
>>>XEM THÊM:Công thức hóa học của giấm là gì? Hướng dẫn cách làm giản dị và đơn giản tận nơi
Có bao nhiêu loại liên kết cộng hóa trị?
1. Liên kết cộng hóa trị có cực
- Một liên kết này sẽ tiến hành tạo thành khi những e dùng chung giữa những nguyên tử không được share như nhau. Điều này chỉ xẩy ra trong trường hợp một nguyên đơn tử có độ âm điện lơn hơn bên mà nó đang share (sẽ có được lực hút mạnh hơn so với những điện từ). Chính vì vậy, kéo theo việc share những electron không được đồng đều.
- Điểm sáng nổi trội: phân tử sẽ nghiêng về phía chứa nguyên tử có độ âm điện thấp hơn, còn phía hơi âm chứa nguyên tử có độ âm điện lơn hơn.
- Thành quả của liên kết này là hợp chất cộng hóa trị được hình thành sẽ có được một thế tĩnh điện.
2. Liên kết hóa trị không cực
- Nó được tạo thành khi những nguyên tử share những electron là đều nhau. Điều này thường xẩy ra với hai nguyên tử có lực tương tự hoặc cùng điện từ. Trong số đó, những giá trị lực điện tử của chúng càng gần thì sức hút càng mạnh.
- Điều đó cùng xẩy ra trong những phân tử khí hay còn gọi là diatomic. Những hạt có độ âm điện lơn hơn sẽ hút e thoát khỏi bên yếu hơn.
3. Liên kết đơn phân tử
- Nó xẩy ra khi hai phân tử đều share một cặp electron duy nhất. Tuy nhiên dạng này yếu hơn và tỷ lệ nhỏ hơn so với liên kết đôi và ba nhưng bù lại nó lại ổn định nhất do có mức độ phản ứng thấp, đồng nghĩa với việc khi bị mất e sẽ ít bị tác động hơn.
4. Liên kết đôi phân tử
- Được gọi cho hiện tượng kỳ lạ hai nguyên tử share hai cặp e lẫn nhau. Nó được mô tả bằng hai tuyến đường ngang giữa hai nguyên tử trong cùng một phân tử. Loại này mạnh hơn so với liên kết đơn nhưng nó kém ổn định hơn.
5. Liên kết ba phân tử
- Là loại kém ổn định nhất trong số những liên kết cộng hóa trị, xẩy ra khi có ba cặp electron được share giữa hai nguyên tử trong một phân tử.
Tính chất của những chất có liên kết cộng hóa trị
- Những chất mà phân tử chỉ có loại liên kết này rất có thể là chất rắn như đường, sắt, lưu huỳnh,… hay chất lỏng như rượu, nước,… hoặc chất khí như clo, cacbonic, hidro,… Những hợp chất chỉ có LKCHT thường có tâm điểm chảy và điểm sôi tương đối thấp, có entanpi hóa hơi cùng nhiệt hạch thấp hơn.
- Ở những chất có cực như đường, ancol etylic,… sẽ tan nhiều trong dung môi có cực như nước. Phần lớn chất không cực như ion,.. tan trong những dung môi không cực như cacbon tetraclorua, benzen,..
Một vài tính chất của liên kết phân tử:
- LKCHT không kéo theo sử hình thành của những e mới mà chỉ rất có thể trao đổi với nhau
- Là những liên kết hóa học rất mạnh tồn tại giữa nhiều nguyên tử
- Thường chứa khoảng chừng 80 kilocalories/ mol (kcal/mol) cho một liên kết
- Sau khoản thời gian được hình thành rất hiếm khi bị phá vỡ một kiểu tự nhiên

Những chất có liên kết cộng hóa trị có tính chất gì
Phân biệt liên kết cộng hóa trị và liên kết ion
Liên kết hóa trị
Liên kết ion
Hình thành giữa hai phi kim loại với độ âm điện giống nhau
Hình thành giữa một yếu tố kim loại cùng một yếu tố phi kim
Có hình dạng xác định
Hình dạng không thắt chặt và cố định
Điểm trung tâm chảy cùng điểm sôi thấp
Điểm trung tâm chảy cùng điểm sôi cao
Độ phân rất thấp và có tính dễ cháy
Có độ phân cực cao và khó cháy
Trạng thái lỏng hoặc khí khi ở nhiệt độ phòng
Trạng thái rắn tại nhiệt độ phòng
Ví dụ: axit clohidric (HCl), metan (CH4)
Ví dụ: acid sulfuric (H2SO4), natri clorua (NaCl)
Sự không giống nhau giữa liên kết hóa trị và liên kết ion
Một vài bài tập vận dụng liên kết cộng hóa trị
Lưu ý:
Cách tìm loại liên kết
- Xác định hiệu độ âm điện x
- Tiếp sau đó so sánh:
x < 0,4 => LKCHT không cực
0,4 ≤ x < 1,7 => LKCHT phân cực
x ≥ 1,7 +> liên kết ion

Một vài bài tập liên quan đến liên kết phân tử
Bài tập 1: Hợp chất nào sau đâu có cả liên kết cộng hóa trị có cực cùng không phân cực?
1. NH4Br
2. H2O2
3. CH4
4. HF
Lời giải:
Đáp án đúng: B
- Do H2O2 có độ âm điện giữa O và H là 1 trong những,4 -> liên kết O-H có cực
- Hiệu số độ âm điện giữa O và O bằng 0 -> liên kết O-O không phân cực
Bài tập 2: Hợp chất nào tiếp sau đây vừa đựng liên kết cộng hóa trị vừa đựng liên kết ion?
1. NaOH
2. NaBr
3. NaNC
4. NaCN
Lời giải:
Đáp án: C
- Liên kết cộng hóa trị giữa nguyên tử N cùng C và liên kết ion giữa Na+ + – NC
Bài tập 3: Liên kết cộng hóa trị có thực chất là:
1. Lực hút tĩnh điện trong số những ion trái dấu
2. Cặp electron dùng chung giữa những nguyên tử
3. Lực tương tác trong số những phân tử
4. Lực tương tác giữa những nguyên tử
Lời giải:
Đáp án: B
Bài tập 4: Cho độ âm điện của oxi và hidro thứu tự là 3,44 và 2,20. Vậy trong phân tử H2O có liên kết hóa học là
1. Ion
2. Cộng hóa trị không phân cực
3. Cộng hóa trị phân cực
4. Tất những những đáp án trên đều sai
Lời giải:
- Ta có hiệu độ âm điện là: 3,44 – 2,20 = 1,24
- Do 0,4 < 1,24 < 1,27 => liên kết cộng hóa trị phân cực
Đáp án đúng: C
Bài tập 5: Độ âm điện của nhôm là 1 trong những,61, còn của lưu huỳnh là 2,58. Vậy liên kết hóa học trong phân tử Al2S3 là:
1. Liên kết ion
2. LKCHT không phân cực
3. LKCHT phân cực
4. Không phải 3 đáp án trên
Lời giải:
- Xét hiệu độ âm điện: 2,58 – 1,61 = 0,97
- Ta thấy: 0,4 < 0,97 < 1,7
=> Liên kết trên là LKCHT phân cực. Đáp án C
Trên đấy là những thông tin trả lời cho thắc mắc liên kết cộng hóa trị là gì cùng tính chất và một trong những bài tập vận dụng cơ phiên bản. Mong rằng, nội dung bài viết đã hỗ trợ những người hiểu hơn về vấn đề này. Nếu còn vấn đề nào thắc mắc cần trả lời, quý người đọc vui lòng liên hệ đến hotline 0826 010 010 hoặc nhắn tin trải qua website vietchem.com.vn để được tư vấn trực tiếp.
